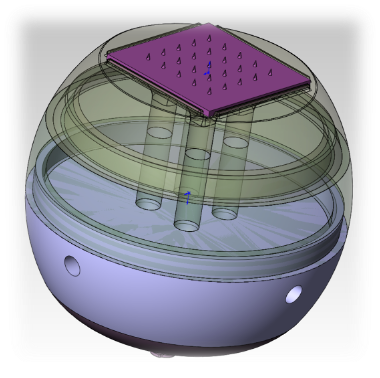
Описание проекта
Носимый экспресс анализатор содержания веществ для формирования персонифицированного профиля человека в целях оптимального медикаментозного воздействия и возможности разработки индивидуальной схемы терапии (on demand drug delivery) в режиме дистанционного обслуживания (телемедицины).
АНАЛИЗ КОНЦЕНТРАЦИИ ВЕЩЕСТВ И МОЛЕКУЛ В ТЕЛЕ ЧЕЛОВЕКА
БЕЗ БОЛИ И КРОВИ ДЛЯ 4П и ТЕЛЕМЕДИЦИНЫ
Существует много быстрых и точных методов анализа состояния человека по составу его крови.
Однако трудность в том, что забор крови связан с весьма болезненной процедурой и посещением медицинского кабинета.
Мы предлагаем решение, которое позволит определять содержание широкого спектра веществ и молекул в Вашем теле с помощью абсолютно безболезненной процедуры.
Ваша кровь не нужна - есть НОВАЯ биоматрица!
Не тратьте Ваше время – сделайте анализ, не выходя из дома!
ПОЛНОЕ НАЗВАНИЕ
Носимый экспресс анализатор содержания молекул и веществ для формирования персонифицированного профиля человека в целях оптимального медикаментозного воздействия и возможности разработки индивидуальной схемы терапии (on demand drug delivery) в режиме дистанционного обслуживания (телемедицины).
ЦЕЛЕВАЯ АУДИТОРИЯ
- нуждающиеся в непрерывной или сложной фармакотерапии, в т.ч. диабет.
- спортсмены, водители, пилоты
- сторонники ЗОЖ и Biohacking
- косметологи и дерматологи
- криминалистика
- работники вредных производств
- малоподвижные или изолированные группы населения
- цифровые Фельдшерско-Акушерские Пункты в федеральной программе «Единый цифровой контур»
ФОРМ ФАКТОР
Существует много носимых мониторов физических параметров тела человека, в том числе с удаленной передачей данных.
Наше устройство УНИКАЛЬНО тем, что оно производит измерение химических параметров организма без боли и использования крови. Дополнительным преимуществом устройства является его микроразмеры, автономность и беспроводной способ передачи данных.
ЦЕЛЬ ПРОЕКТА
Создание модульной платформы, которая обеспечит возможность проведения экспресс анализов с использованием широкой гаммы современных биосенсоров, и передачу результатов в Национальную Базу Медицинских Знаний и Единый Цифровой контур Федеральной программы национального проекта «Здравоохранение».
Проект соответствует концепции проекта-маяка НТИ HEALTHNET: ПЕРСОНАЛЬНЫЕ МЕДИЦИНСКИЕ ПОМОЩНИКИ и абсолютно новой модели здравоохранения - 4П-медицина. Свое название она получила от четырех основополагающих принципов: персонализации, предикции, превентивности и партисипативности. 4П-медицина направлена на то, чтобы выделить факторы риска, определить предрасположенность пациента к тем или иным болезням и предотвратить их.
ПОЧЕМУ ЭТО ВОЗМОЖНО
Биохимическая информация об организме чаще всего поступает из анализа крови, которая составляет всего 6% жидкостей организма, но ценную информацию можно также найти в других жидкостях организма, которые традиционно трудно получить. Кожная интерстициальная жидкость (ISF), которая циркулирует между клетками в тканях организма, может обеспечить новый подход к получению диагностических биомаркеров и выявлению потенциальных токсинов. Поскольку ISF не сворачивается, как кровь, экстракция на основе микроигл может предложить новый подход для непрерывного мониторинга уровня глюкозы и других ключевых показателей здоровья.
Система на основе микроигл может стать, например, менее инвазивной альтернативой имплантируемым датчикам глюкозы, позволяя чувствительным компонентам оставаться на поверхности кожи.(32-36)
ISF на самом деле происходит из крови—он вытекает из капиллярных сетей, чтобы доставлять питательные вещества клеткам в тканях организма. Этот прямой контакт и связь с клетками позволяют ISF собирать биохимические данные, касающиеся состояния здоровья этих тканей.
ДОРОЖНАЯ КАРТА
ХЭЛСНЕТ - Рынок персонализированных медицинских услуг и лекарственных средств, обеспечивающих рост продолжительности жизни, а также получение новых эффективных средств профилактики и лечения различных заболеваний
ЧТО БУДЕТ СДЕЛАНО НА ПРИВЛЕКАЕМЫЕ СРЕДСТВА?
Разработан и изготовлен прототип компактного автономного устройства для безболезненного оперативного забора и анализа биоматериала из эпидермиса с определением содержания 2-3- различных медикаментов или молекул.
Разработан прототип новой технологическая платформы, позволяющей контролировать прием лекарственных средств;
АКТУАЛЬНОСТЬ ПРОБЛЕМЫ
В последние годы осложнения лекарственной терапии все больше осознается как чрезвычайно важная проблема, имеющая медицинский, социальный и финансовый аспект [2; 4; 20; 21; 26]. Улучшение качества оказания медицинской помощи относится к основным задачам здравоохранения на современном этапе его развития.
Для предупреждения лекарственных осложнений во многих странах организованы специальные центры по контролю безопасности лекарств. Всемирная организация здравоохранения (ВОЗ) в рамках международной программы проводит мониторинг по безопасности лекарственных средств, в которой участвуют более 100 стран. В базе данных ВОЗ имеется около 5 млн. сообщений о неблагоприятных побочных реакциях (НПР) на прием лекарственных препаратов.
В отличие от зарубежных стран, официальные статистические данные о серьезных последствиях применения фальсифицированных лекарственных средств (ФЛС) в российской практике отсутствуют: врачи не склонны усматривать наличие связи между НПР или ухудшением состояния пациента с качеством применяемых ЛС и ошибками фармакотерапии [1; 5; 9; 11;12; 16; 19].
Проблема 1. Низкая эффективность затрат на медикаментозное лечение без учета индивидуальной восприимчивости пациента.
Проблема 2. Экономические и социальные потери от ошибок дозировки без учета индивидуальной восприимчивости пациента.
Проблема 3. Социально-экономические и физиологические преграды формирования цифрового профиля пациента классическими методами.
ОЖИДАЕМЫЙ ЭФФЕКТ
- Снижение фармакологической нагрузки за счет уменьшения дозировок обезболивающих препаратов по сравнению со стандартной фармакотерапией;
- Повышение эффективности лечения больных по сравнению с текущими практиками;
- Сокращение расходов средств на медикаментозное лечение пациентов медицинских учреждений;
- Сокращение числа случаев передозировки лекарственными препаратами;
- Сокращение сроков нетрудоспособности по болезни;
Рынок
По прогнозам, к 2025 году объем глобального рынка диагностики в медицинских учреждениях достигнет 50,6 млрд долларов США по сравнению с 29,5 млрд долларов США в 2020 году, что в среднем составит 11,4% в течение прогнозируемого периода. Технологические достижения в области устройств POC, рост заболеваемости инфекционными заболеваниями и увеличение инвестиций ключевых игроков являются ключевыми факторами, стимулирующими рост рынка диагностики в пунктах оказания медицинской помощи POC (Point of Collection).
Молекулярная Диагностика-это самый быстрорастущий сегмент более широкого рынка диагностики. Ожидается, что рынок МД вырастет с 8,5 миллиарда долларов в настоящее время примерно до 20 миллиардов долларов к 2030 году.
Движущей силой отрасли является очень короткий срок проведения высококачественных испытаний. Молекулярное тестирование POC помогает врачам повысить качество медицинской помощи, интегрируя быстрые решения по диагностике и лечению при первом посещении пациента вместо часов и дней.
По продукту сегмент мониторинга глюкозы, как ожидается, будет занимать наибольшую долю рынка (39%) в течение прогнозируемого периода.
Большая доля этого сегмента объясняется такими факторами, как значительное внедрение новых технологий исследований, технологические достижения, растущая база пациентов с диабетом и растущее предпочтение домашнего тестирования на глюкозу. Были проведены клинические исследования, которые показали репрезентативность ISF для определения уровня глюкозы.
Портативное оборудование стремительно занимает быстрорастущие рынки POCT и молекулярной диагностики для персонализированного и децентрализованного цифрового здравоохранения.
По прогнозам, объем мирового рынка ветеринарной диагностики в пунктах оказания медицинской помощи достигнет 2,4 миллиарда долларов США к 2025 году с 1,4 миллиарда долларов США в 2019 году, в среднем на 8,9%.
Децентрализация того, что традиционно было централизованным лабораторным тестированием, играет ключевую роль. Приближение МД к пациенту дает преимущество обнаружение болезненного состояния до того, как у пациента появятся симптомы. Наличие устройства POCТ в клинике означает, что результаты будут быстрыми, и терапия может быть назначена до дальнейшего прогрессирования заболевания. При инфекционных заболеваниях ранняя диагностика может облегчить боль пациента, сократить время выздоровления и замедлить или остановить распространение заболеваний. В случае онкологии и пренатального тестирования ранняя диагностика может спасти жизнь.
ТЕХНОЛОГИЧЕСКОЕ РЕШЕНИЕ
- Создание микро-устройства для быстрого и безболезненного извлечения и хранения рабочих объемов биоматериала
- Разработка форм фактора и протокола обмена биоматериалом с биосенсорами 10 наиболее критичных к дозировке медикаментов.
- Разработка системы записи, хранения и визуализации результатов анализа.
- Разработка технологии модульной сборки конечного устройства.
- Разработка протокола и механизма передачи результатов анализа в федеральную сеть сбора первичных биомедицинских данных «Национальная база медицинских знаний» *
Базовая методология реализации проекта - создание модульной 3D конструкции устройства, на основе достижений в областях:
- 3D сборки микроэлектронных устройств;
- Биосенсоров веществ в микрообъемах;
- MEMS технологии в микрофлюидике**.
*«Национальная база медицинских знаний» (НБМЗ) заявлена как важнейший шаг в реализации стратегической дорожной карты «Искусственный интеллект в медицине. Цифровое здравоохранение». Инициатива поддержана Национальной ассоциацией Заслуженных Врачей России, Российской венчурной компанией (РВК), Агентством стратегических инициатив (АСИ), а также Национальным Агентством Социальных Коммуникаций (НАСК).
**междисциплинарная наука, описывающая поведение малых (порядка микро и нанолитра) объёмов и потоков жидкостей.
ПРЕДПОСЫЛКИ ВОЗНИКНОВЕНИЯ ИДЕИ
Государство оказывает бесплатную медицинскую помощь населению, но несет избыточные затраты, связанные с длительным поиском эффективного медикамента традиционным методом «перебора». Это увеличивает время нетрудоспособности сотрудников предприятий, приводит к осложнениям.
Мониторинг содержания лекарственных препаратов является динамичной научно-клинической областью медицинских знаний; играет важную роль в решении задач, возникающих в результате постоянного увеличения ассортимента лекарственных препаратов, при применении которых нередко возникают побочные реакции [6; 8; 13; 15; 27; 28].
Проектируемое устройство позволит повысить эффективность фармакотерапии с ограничением факторов риска развития НПР. Результаты исследований могут использоваться в качестве предикторов ответа на проведение фармакотерапии с учетом полиморбидного фона, возраста пациента, состояния функционирования органов метаболизма и экскреции, формы и периода заболевания, особенностей взаимодействия лекарств.
Применение рекомендованных информативных факторов риска позволит прогнозировать исход фармакотерапии, повысить эффективность и безопасность лечения. Разработанные и внедренные алгоритмы взаимодействия участников системы контроля будут способствовать внедрению современных стандартов лечения и повышению качества медицинской помощи.
В основу современной рациональной фармакотерапии положены следующие критерии: соответствие выбора ЛС действующим стандартам; адекватность дозы, режима приема, лекарственной формы путям введения ЛС; обоснованность использования ЛС в комбинированной терапии; возможность предупреждения побочных эффектов ЛС; доказанная эффективность и безопасность ЛС; достаточный опыт применения ЛС; благоприятное соотношение стоимость/эффективность ЛС (экономичность).
Лекарственные осложнения занимают 4 место в США по частоте летальных исходов после смертности от сердечно-сосудистых заболеваний, злокачественных опухолей и инсультов, и уносят более 100 000 жизней. Данные мета—анализа проведенного в США, указывают, что побочные эффекты лекарств занимают 4-6 место в структуре причин летальности среди госпитализированных пациентов. В США до 140 тыс. человек погибают ежегодно в результате осложнений лекарственной терапии [17; 22; 23; 24; 25; 29; 30].
Н.В. Иванова (2004) сообщает о том, что расходы на лечение осложнений лекарственной терапии, обусловленных различными типами врачебных ошибок (игнорирование анамнестических данных о непереносимости лекарственных средств в прошлом; неоправданный выбор лекарственных средств; игнорирование противопоказаний к применению; ошибки дозирования препарата; назначение лекарственных средств без учета их взаимодействия) составляют 10,7% расходов в общей структуре затрат на лекарственно-обусловленную заболеваемость и смертность [3; 7; 14; 18; 31].
Ссылки
- Врачебные ошибки как причина осложнений лекарственной терапии / В.К. Лепахин [и др.] // Качественная клиническая практика. - 2002. — № 1. -С. 71-77.
- Иванова; НЛЗ; Структура экономических затрат, обусловленных осложнениями лекарственной терапии / Н.В. Иванова // Экономика здравоохранения. - 2004. - № 1. - С. 34-36.
- Истратов, C.IO. Взаимодействие лекарственных средств / С.Ю. Истратов, Е.В. Брайцева, И.Р. Вартанян // Новая аптека. - 2000. - № 9. - С. 34-38.
- Итоги государственного контроля качества лекарственных средств, мониторинга безопасности лекарственных препаратов, контроля проведения клинических исследований лекарственных препаратов за 2010 год [Электронный ресурс]. - Режим доступа: Федеральная служба по надзору в сфере здравоохранения и социального развития. URL: http: //www.roszdravnadzor.ru/medicine... (дата обращения 25.02.11), свободный.
- Кантер, Э.И. О случайных «медицинских» отравлениях после внутривенных и подкожных введений лекарств: дисс. ... канд. мед. наук /
- Клевцова, JT. Безопасность медикаментозной помощи: проблема мониторинга / Л. Клевцова // Московские аптеки. - 2003. - № 5. - С. 2334.
- Клинико-фармакологические аспекты взаимодействия лекарственных средств с позиции персонализированной медицины / под ред. В.Г. Кукеса [и др.].-М., 2012.-С. 7-17.
- Косенко, В.В. Деятельность Росздравнадзора по обеспечению качества лекарственных средств / В.В. Косенко // Вестник Росздравнадзора. - 2009 -№3. - С.4-13.
- Косенко, B.B. Фальсифицированные лекарства - глобальная проблема / В.В. Косенко, A.B. Быков, А.П. Мешковский // Вестник Росздравнадзора. 2009. — № 3. - С. 14-26.
- ххххххххххххххххххх
- Косенко, В.В. Организация системы мониторинга безопасности зарегистрированных лекарственных препаратов в Российской Федерации / В.В. Косенко, C.B. Глаголев // Вестник Росздравнадзора. - 2011. - №6. - С. 3139.
- Красильников, А.П. Ятрогении и безопасность медицинской помощи / А.П. Красильников // Медицинские новости. - 1996. - №4. - С. 3-10.
- Культура безопасности лекарственной терапии / A.J1. Хохлов [и др.]. -Ярославль: Ремдер, 2011.-169 с.
- Лепахин, В.К. Фармакоэпидемиологическое исследование нежелательных реакций, связанных с взаимодействием лекарственных средств / В.К. Лепахин, A.C. Казаков, A.B. Астахова // Клиническая фармакология и терапия. - 2013. - №22 (4). - С.92-96.
- Окунь, Т.В. Проблема мониторинга безопасности лекарственных средств / Т.В.Окунь, Н.В. Верлан, Г.Г. Паисова // Сибирский медицинский журнал. - 2011. - № 6. - С.204-206.
- Сбоев, Г.А. Технологии гармонизации систем госрегулирования, регистрации, контроля производства и применения лекарственных средств / Г.А. Сбоев, В.Л. Багирова, И.И. Краснюк // Экономический вестник фармации. -2003. -№ 10.-С. 11-22.
- Списер, Ж.М. Европейская система допуска активных фармацевтических субстанций и вспомогательных веществ к использованию в производстве лекарственных средств / Ж.М. Списер // Вестник Росздравнадзора. - 2010. - № 6. - С. 26-29.
- Сычев, Д.А. Клинико-фармакологические подходы к решению проблемы полипрагмазии у пожилых пациентов в условиях многопрофильного стационара / Д.А. Сычев, К.С. Данилина, В.А. Отделенов // Клиническая фармакология и терапия. - 2013. - Т. 22, № 2. - С. 87-92.
- Топорков, A.A. О мерах по предотвращению поступления в обращение фальсифицированных лекарственных средств / A.A. Топорков // Новая аптека. - 2002. - № 5. - С. 33-38.
- Указ Президента РФ от 12.05.2009 г. «О стратегии национальной безопасности Российской Федерации до 2020 года» [Электронный ресурс] // Совет Безопасности Российской Федерации [сайт]. URL: http:/Av\v\v.scrf.gov.ru/documents/99.html (дата обращения 13.11.2010).
- Федеральный закон от 21.11.2011 № 323-ФЭ «Об основах охраны здоровья граждан в Российской Федерации».
- Adverse Drug Events: Substantial problem but magnitude uncertain // US General Accounting Office. - 2000. - February. - P. 1-12.
- Cornish, P.L. Unintended medication discrepancies at the time of hospital admission / P.L. Cornish, S.R. Knowles, R. Marchesano et al. // Arch. Intern. Med. - 2005. - Vol. 165, N 4. - P. 424-429.
- FDA Alerts U.S. Residents to Recall of Counterfeit «Lipitor» Sold in the Un-ated Kingdom : FDA news release (July 29, 2005) // U. S. Food and Drug Administration [web-site], URL: http://www.fda.gov/NewsEvents/... /PressAnnouncements/2005/ucm 108469.htm, (October 12, 2009).
- FDA Announces New Initiative to Protect U.S. Drug Supply Through the use of Radiofrequency Identification Technology : FDA news release (November 15, 2004) // U. S. Food and Drug Administration [web-site], URL: http://\vww.fda.gov/NewsEvents... 8372.htm, (January 03, 2010).
- Muehlberger, N. ADRs Monitoringt Pharmacoepidemiology and drug safety / N. Muehlberger, S. Schneeweis, J. Hasford. - 1997. - Vol. 6, Suppl. 3. - P. 7177.
- Paulsen-Sorman, U. Market Surveillance of Centrally authorised Products / U. Paulsen-Sorman, R. Wanko, J.-M. Spieser // Regulatory Affairs Journals. -2000.-Vol. 11.-P. 1234- 1246
- UK Department of Health. An organization with a memory. - London, 2000. -December. - 108 p.
- Quality of Care Patient Safety // WHO. - 2002. - Resolution EB. - № 109. -P. 16.
- Quality of Health Care in America Committee. The Institute of Medicine Report on Medical Errors: Misunderstanding Can Do Harm / C.R. William [et al.] // Med. Gen. Med. - 2000. - September 19. - 10 p.
- Questions and answers on the recall of Vimpat 15mg/ml syrup (lacosamide) (21 July 2011) // European Medicines Agency [web-site], URL:http://www.ema.europa.eu/docs/... 2011/07AVC500109225.pdf (5 September, 2011).